腫瘍内ワクチン「iVAC」:がんを“見える化”するトロイの木馬戦略
免疫療法が効きにくい「免疫コールド腫瘍」を、内側から“露出”させて免疫に見つけさせる——そんな発想の腫瘍内ワクチンが、がん治療の次の選択肢として注目されています。
北京大学チームが報告した「腫瘍を隠れさせない」ワクチン
中国本土の北京大学で化学生物学を研究する彭鵬(Peng Chen)教授のチームは、腫瘍内に投与する「トロイの木馬」型ワクチンについて、学術誌Natureで報告しました。狙いは、がんを外から叩くだけでなく、腫瘍細胞自身に“正体を提示させる”ことです。
ここ数年、手術・化学療法・放射線療法に加えて、免疫の力を引き出す免疫療法が広がってきました。一方で、免疫療法が効きにくい患者が一定数いることも知られています。今回の研究は、その難所に別方向からアプローチします。
なぜ免疫療法が効かない腫瘍があるのか
免疫の主役の一つがT細胞です。T細胞は異常な細胞を見つけて排除する役割を担い、がん細胞の変異によって生じる「異常なタンパク質断片(抗原)」は、本来なら目印になります。
それでも腫瘍が見逃される背景には、免疫から逃げる仕組みがあります。研究チームが焦点を当てた代表例がPD-L1です。腫瘍細胞がPD-L1を発現すると、T細胞への抑制シグナルとなり、攻撃が鈍ることがあります。このため、たとえば非小細胞肺がんなどでは、既存の免疫療法が十分に効かないケースが生じ得る、とされています。
鍵は「PD-L1を壊す」だけでなく「抗原を並べさせる」こと
チームはこれまで、標的タンパク質分解(狙ったタンパク質を細胞内で分解させる)技術に取り組み、2021年にはGlueTACを開発しました。そこからさらに改良を重ね、「抗体を強くする」だけでは届きにくい臨床課題に向き合ったといいます。
彭氏は「抗体の結合を強めたり、標的をより強く抑えたりするだけでは、現実の臨床問題は解決しない。患者によって反応が異なり、腫瘍の多様性も大きい」と強調しています。
iVACのしくみ:腫瘍の内側で起きる3つの連動
約4年の改良を経て開発されたのが、キメラ型の腫瘍内ワクチンiVACです。特徴は「腫瘍細胞が自分の抗原を処理し、表面に提示する」流れを強く促す点にあります。
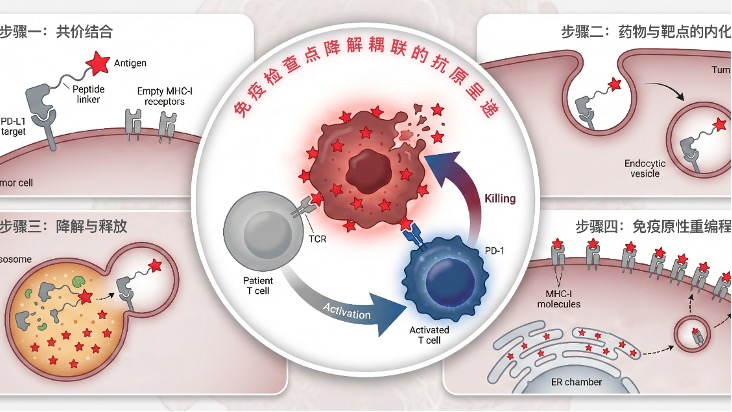
iVACは分子量がおよそ18kDaと小さく、固形腫瘍へ入り込みやすい設計だとされています。動きは大きく3段階です。
- PD-L1に結合する:先端の共有結合性ナノボディがPD-L1(腫瘍の「撃たないで」シグナル)に結合します。
- 細胞内へ引き込ませる:結合後、複合体ごと腫瘍細胞に取り込ませます。
- リソソームで分解し、目印を提示させる:細胞のリサイクル施設にあたるリソソームへ運ばれ、PD-L1が分解されます。同時に、抗原断片が処理され、細胞表面に「識別タグ」のように提示されやすくなります。
つまりiVACは、免疫をただ「活性化する」より一歩踏み込み、腫瘍側の隠れ方(見えにくさ)そのものを崩すことを狙った設計と言えます。
「腫瘍内投与」が示す現実的な問い
腫瘍内ワクチンという形は、標的を腫瘍局所に集めやすい一方で、どの腫瘍に、どのような投与設計が可能かといった運用面の問いも伴います。免疫コールド腫瘍の「見えにくさ」をどう崩すかは、2026年のがん免疫領域でも引き続き大きなテーマです。
今回の報告は、PD-L1という免疫回避の鍵を“内側へ引きずり込んで分解する”発想と、抗原提示を促して標的を浮かび上がらせる設計が、同じ流れで結び付けられることを示しました。今後、どのがん種で、どのような条件下で臨床的な意味を持つかが、次の焦点になりそうです。
Reference(s):
cgtn.com








